La ciencia detrás de las terapias avanzadas
El proceso de producción de las terapias avanzadas es altamente complejo y requiere instalaciones especializadas y procesos altamente regulados. Cada tipo de terapia presenta distintos retos en su producción. Según la Agencia Europea de Medicamentos (EMA), los medicamentos basados en terapias avanzadas se pueden diferenciar en [1]:
- Terapias celulares: contienen células o tejidos que han sido manipulados para cambiar sus características biológicas o que se utilizan con una función diferente a la original en el cuerpo. Un ejemplo es la aplicación de células madre, que tienen el potencial de regenerar tejidos dañados.
- Terapias génicas: incluyen genes que producen un efecto terapéutico, profiláctico o diagnóstico. Funcionan insertando genes “recombinantes” en el organismo, generalmente para tratar enfermedades genéticas, cáncer o patologías crónicas. Las terapias más comunes utilizan vectores virales para introducir el material genético en las células del paciente.
- Ingeniería tisular: combina células con materiales biocompatibles para formar estructuras tridimensionales que pueden reparar, regenerar o reemplazar tejido humano.
Uno de los mayores desafíos en la producción de estas terapias es que aún dependen en gran medida de procesos manuales. Aunque la metodología manual es válida en las primeras fases de desarrollo, dificulta la escalabilidad, la estandarización de los procesos y el control de costes. Además, un alto grado de manipulación manual aumenta el riesgo de variabilidad, contaminaciones y errores humanos.
Ensayos clínicos y terapias aprobadas
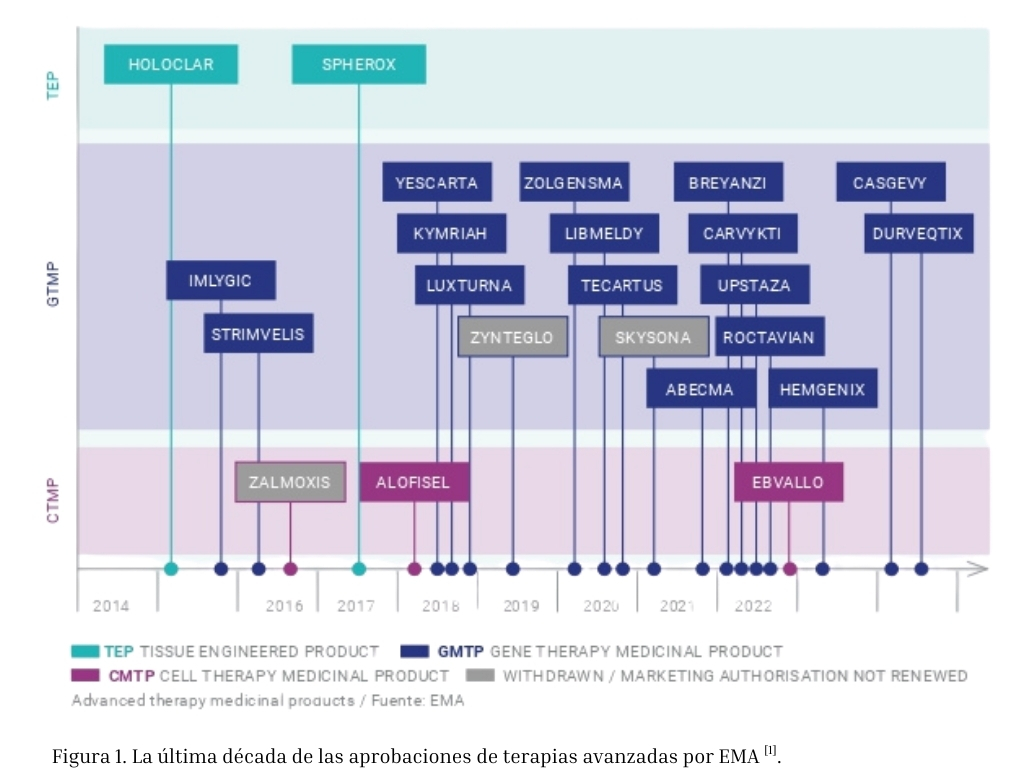
El número de ensayos clínicos relacionados con terapias avanzadas ha aumentado significativamente en los últimos años. Según la Sociedad Americana de Terapias Génicas y Celulares (ASGCT), actualmente hay más de 4.000 terapias celulares y génicas en desarrollo. Sin embargo, a pesar de este crecimiento, solo 100 han sido aprobadas globalmente para uso clínico. En cuanto a los productos de ingeniería tisular, únicamente 8 han recibido autorización para su comercialización [2].
Esta brecha entre innovación y aprobación se debe, principalmente, a los altos estándares regulatorios, los elevados costes de investigación y el prolongado tiempo de desarrollo. No obstante, a pesar de estos obstáculos, las aprobaciones por parte de la FDA y la EMA reflejan el enorme progreso alcanzado en los últimos años y el papel fundamental de estas terapias en la medicina moderna.
Barreras para la disponibilidad y accesibilidad
A pesar de los avances en la investigación y desarrollo, y de las oportunidades que ofrecen estas terapias, existen varios obstáculos que limitan su acceso a la población.
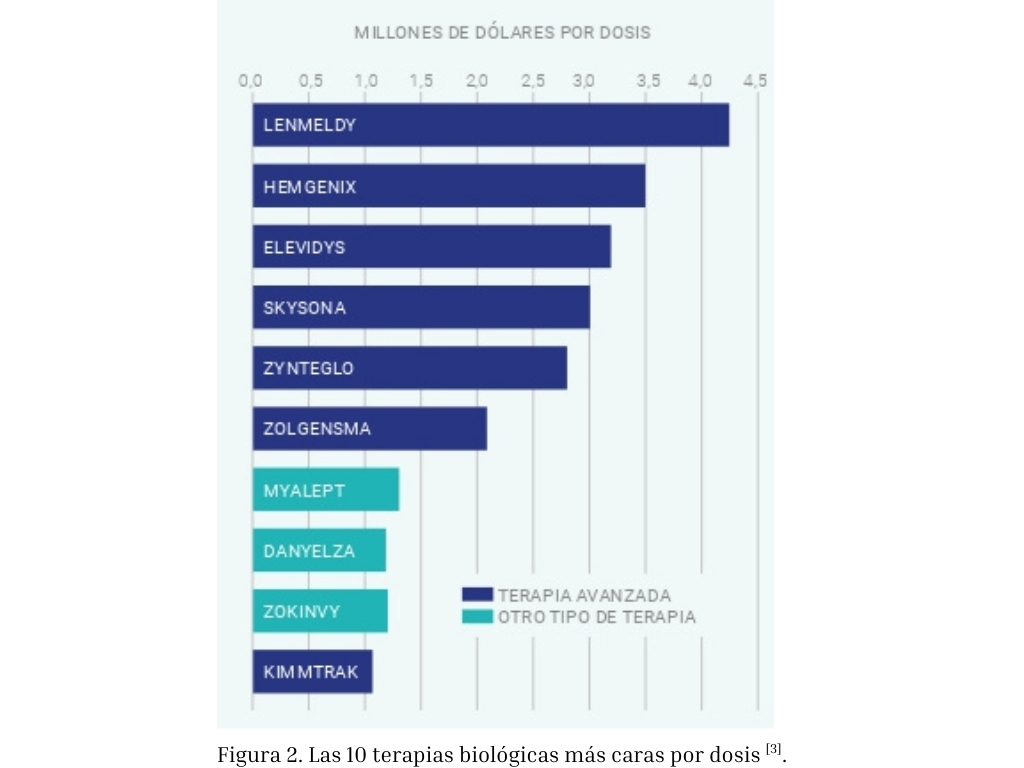
Uno de los principales desafíos es su alto coste por dosis. La producción de estas terapias requiere instalaciones especializadas, materiales de alta calidad y procesos de fabricación complejos y altamente manuales, que encarecen el precio del producto final. El precio de las terapias avanzadas puede suponer varios millones de dólares por paciente, lo que plantea interrogantes sobre su disponibilidad para muchos pacientes y sistemas de salud a largo plazo.
Estos elevados costes también afectan a las empresas que desarrollan estas terapias. Un ejemplo es el caso de bluebird bio, que pasó de tener tres terapias valoradas en 10 billones de dólares a venderlas por 30 millones de dólares [4], reflejando la dificultad de recuperar la inversión en este sector.
Además, las instalaciones necesarias para este tipo de producción son costosas y requieren tecnología y personal altamente especializado. La falta de infraestructura adecuada y la limitada capacidad para producir estos tratamientos a gran escala pueden retrasar su disponibilidad para los pacientes. Finalmente, la infraestructura para la distribución y administración de terapias avanzadas sigue siendo insuficiente, especialmente en regiones fuera de los países más desarrollados. Esto impide que una parte de la población mundial tenga acceso a estas innovaciones terapéuticas.
Reducir costes y facilitar acceso
Para superar estos obstáculos y garantizar mayor accesibilidad a estas terapias revolucionarias, es necesario implementar:
- Automatización de la producción: Incorporar tecnologías de automatización en la producción de células y materiales biológicos podría reducir el tiempo y los costes de fabricación. Además, disminuiría los riesgos asociados a la manipulación manual.
- Diseño de plantas especializadas: Actualmente, la producción de terapias avanzadas está limitada a un número reducido de plantas especializadas o depende de la externalización de los servicios, lo que aumenta su precio. También es importante destacar que gran parte de las terapias avanzadas, como las CAR-T, se producen en infraestructuras especializadas dentro de hospitales y centros de investigación, lo que dificulta su escalado a nivel industrial. Con mayor financiación privada, se podría asegurar la expansión global de la infraestructura de producción y garantizar una mayor disponibilidad de estos medicamentos.
- Colaboración público-privada: Una mayor cooperación entre gobiernos, empresas y el sector académico en investigación y desarrollo de estas terapias podría reducir los costes de producción y distribución.
- Colaboración internacional en infraestructura: Establecer centros de producción globales y armonizar las regulaciones internacionales facilitaría el acceso a estas terapias en distintas regiones del mundo.
Conclusiones
Las terapias avanzadas representan una de las mayores promesas para el tratamiento de enfermedades graves y complejas. No obstante, los elevados costes de producción, los desafíos en escalabilidad y las barreras regulatorias siguen limitando su disponibilidad global.
El futuro de estas terapias dependerá del desarrollo de nuevas tecnologías de automatización, de modelos de financiamiento innovadores y de una infraestructura adecuada para su producción y distribución.
Con los avances en ciencia y tecnología, se espera que estas terapias dejen de ser un privilegio y se conviertan en un estándar accesible para todos.
Klinea es una empresa especializada en ingeniería biofarmacéutica y procesos biológicos. Su labor se centra en brindar asesoramiento técnico y estratégico que facilite a las organizaciones del sector la disponibilidad de sus productos para un mayor número de pacientes, optimizando sus procesos y asegurando estándares de calidad.
Descarga sugerida:
Artículo escrito por:
Andrea Jordà y Jordi Gibert
Ingeniera de Proyectos y Responsable de la Unidad de Biotecnología, respectivamente
Klinea Biotech & Pharma Engineering